欧盟GMP检查:从查询途径到检查趋势分析
2023-10-10 10:14:00在这篇文章中,我们将一一探讨这些问题,帮助您更好地了解欧盟的GMP检查现状。
EudraGMDP介绍
-
生产和进口许可(Manufacturing and import authorisations) -
GMP证书(Good Manufacturing Practice (GMP) certificates.) -
GMP不符合性声明(Statements of non-compliance with GMP) -
第三国的GMP检查计划(GMP inspection planning in third countries) -
批发分销许可(Wholesale Distribution Authorisations) -
GDP证书(Good Distribution Certificates (GDP)) -
GDP不符合性声明(Statements of non-compliance with GDP) -
EEA人用活性物质制造商、进口商和分销商注册(Registration of manufacturers, importers and distributors of active substances for human use located in the EEA)
下面我们将重点介绍一下GMP certificates和Statements of non-compliance with GMP。
GMP证书和GMP不符合性声明



Part 2:与本NCS相关的制造商的活动;
根据本次检查的范围,选择模块中对应内容,针对人用药品、兽用药品、临床试验用药三个部分,包括的模块有:无菌产品、非无菌产品、生物制品、包装、质量控制等,对于进口药品也有进口质量控制检测和批放行(Batch certification of imported medicinal products)等对应选项,如没有列举的内容,需要在“Other”中补充。

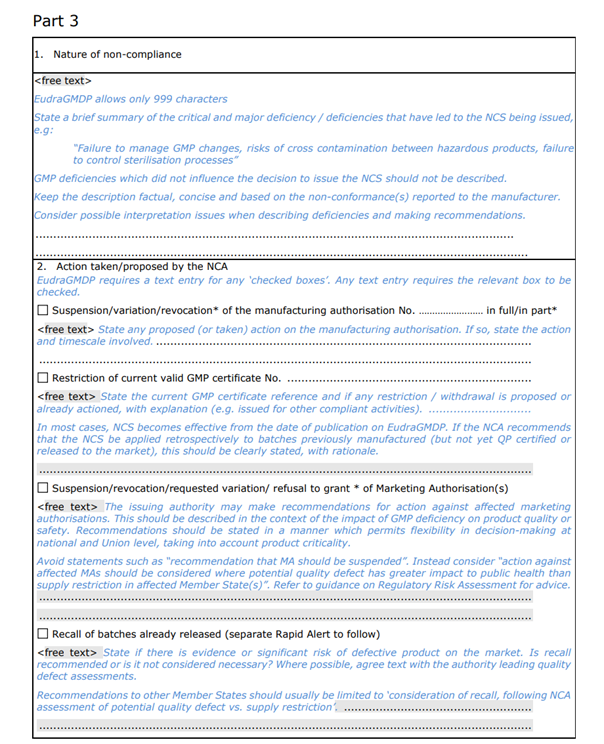
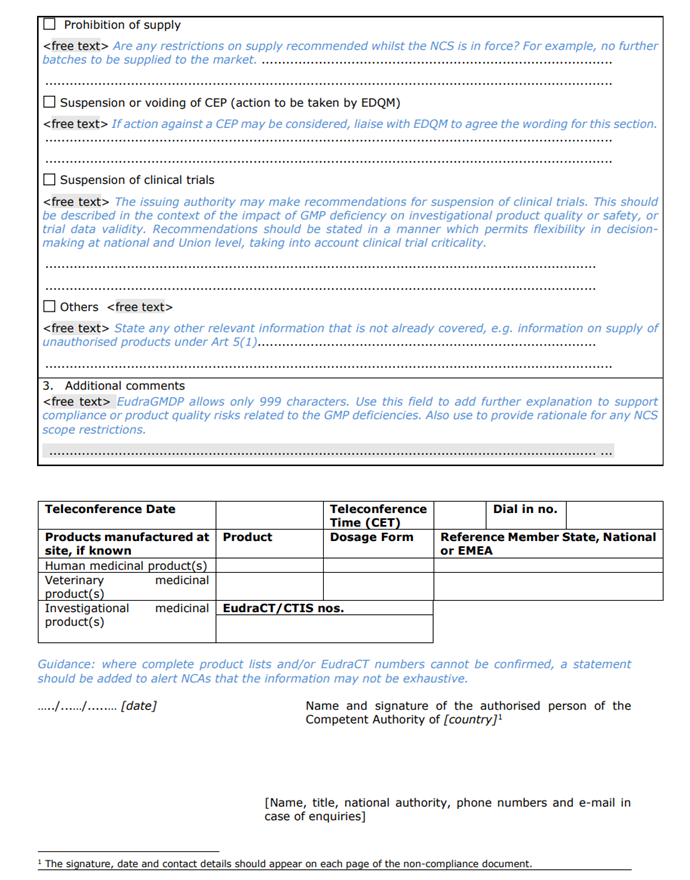
Part 3:不符合项目的说明及官方所要采取的措施;
声明中仅概括了导致本次NCS的关键(critical)和主要(major)缺陷,包括缺陷的数量及简单描述,并未详细的描述具体如何违反GMP。NCA(National Competent Authorities)已采取或建议采取的行动,包括撤销/变更/暂停生产许可、GMP证书、上市许可,中止CEP证书,中止临床试验等情况。
通过欧盟GMP检查企业的缺陷项并未包括在EudraGMDP中,官方会不定期的发布和总结,例如EDQM在2019发布的2006~2018检查和缺陷趋势概况文件(EDQM inspections and trends of deficiencies Overview 2006 to 2018),这份文件中就包括2006~2018年API检查及缺陷分析,大家可以在网上自行查询。
2017~2023年EU GMP检查数据分析
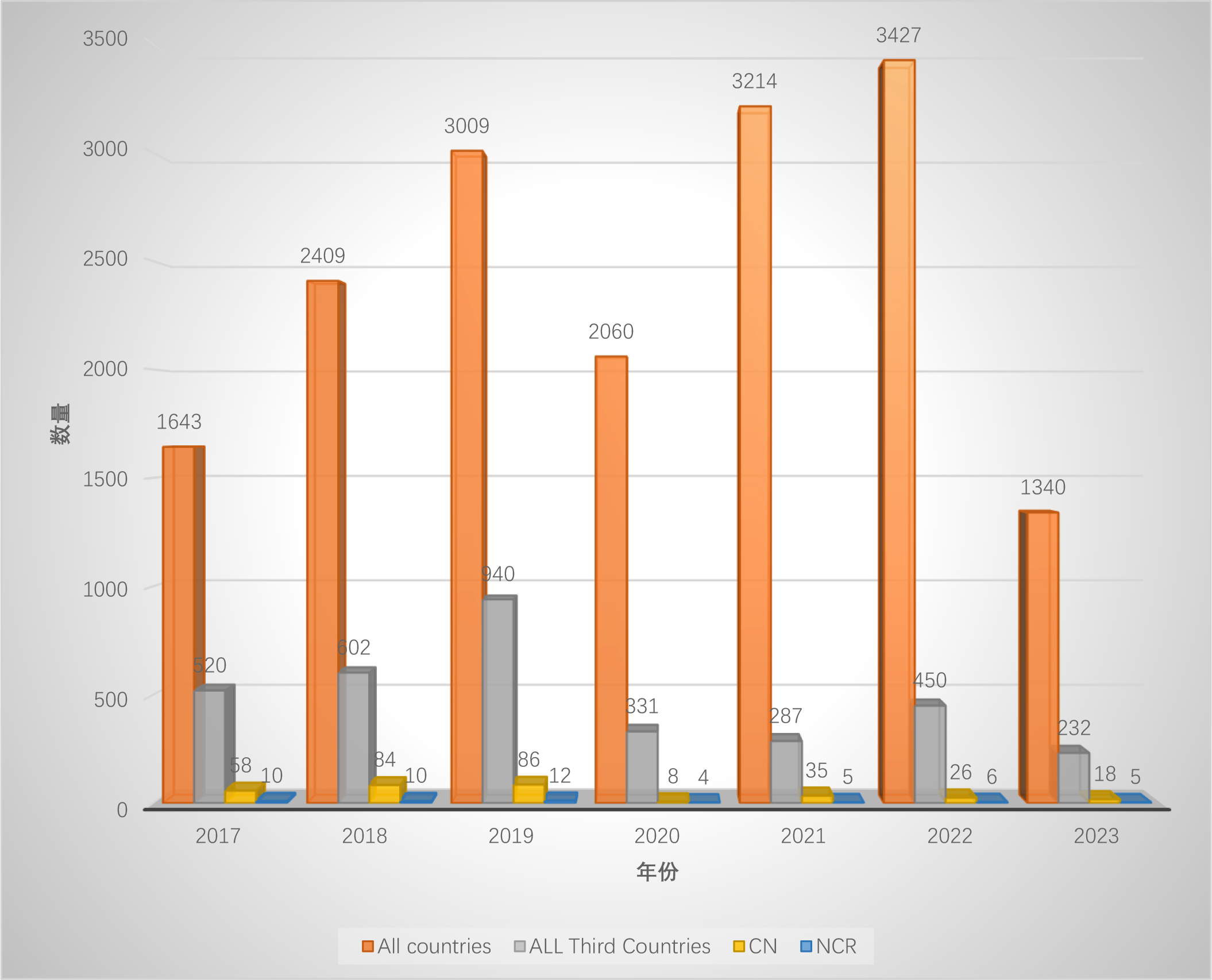
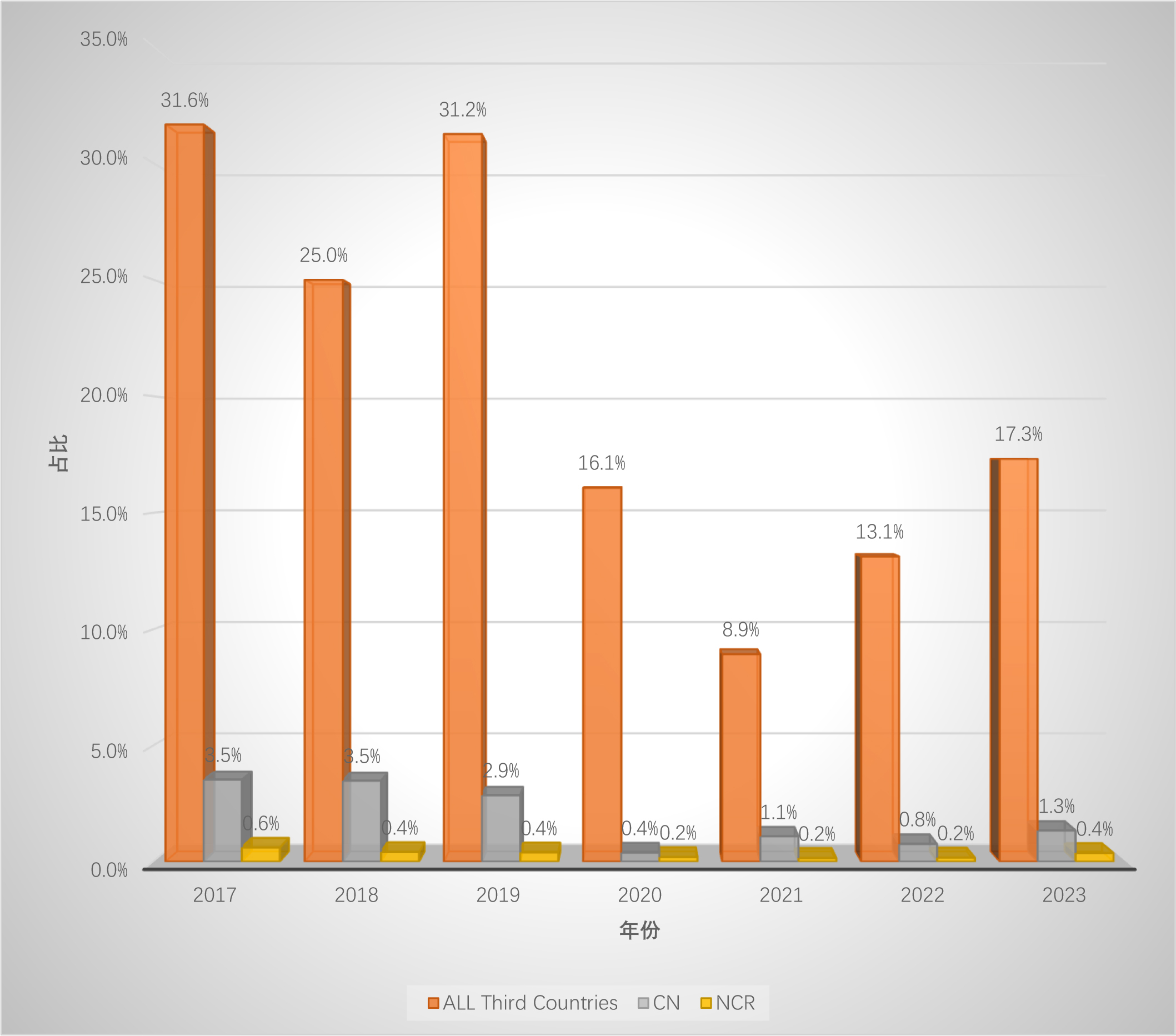
制作了两份图表来对比,图一为不同年份及对应的检查数量,图二是不同年份第三国检查数量、中国检查数量以及发布的不符合声明数量的占比。
如果我们假设检查官都会在检查完成后90天才登记在数据库中,那么2023年的数据刚好是6个月,可以代表2023年一半的检查量。
-
考虑到2020年的特殊情况,2017年至2022年,总的检查数量逐年攀升,但2023年却熄火了,这是为什么? -
2020年以来,虽然开启了远程检查的模式,但是欧盟在第三国的检查总量远低于2017~2019年;原因可能是:新冠期间欧盟发布了“QUESTIONS AND ANSWERS ON REGULATORY EXPECTATIONS FOR MEDICINAL PRODUCTS FOR HUMAN USE DURING THE COVID-19 PANDEMIC”,其中描述了在EEA以外生产的API和制剂的GMP证书有效期延长至2022年底,后续又在EMA官网上写到延长至了2023年底。 -
我们都以为2023年欧盟在包括中国在内的第三国的检查数量会暴增,结果却并没有。如果考虑是因为在EEA以外生产的API和制剂的GMP证书有效期延长至2023年底,那么2023年在中国以及第三国的检查数量将与2022年相近,或可做解释。
仁者见仁,各位看官对这些数据有何看法?
-
EU GMP差距分析
-
质量体系提升
-
专题培训
-
模拟审计
-
迎检准备
-
现场陪检及翻译
-
缺陷关闭指导
在下一期的文章中,我们计划讨论欧盟近年来发布的GMP不符合性声明,研究了解这些声明中究竟涉及了哪些缺陷,以及是什么原因导致了检查未通过。我们欢迎各位继续关注,共同学习,共同进步。
策划:魏巍
编写:王亚蕊











